Introducción

Uno de los
principales atractivos de las Islas Galápagos es su
biodiversidad única en el mundo que la ha convertido desde
1978 en Patrimonio Natural de la Humanidad según la UNESCO.
Con respecto a la diversidad florística del archipiélago,
está constituída por 560 especies de plantas nativas, y
de éstas 175 especies (32%), son endémicas y abarcan
236 taxones (Tye, 2002). Entre estos taxones se encuentran inclusive
géneros que son endémicos de las islas:
Darwiniothamnus, Lecocarpus, Macraea y Scalesia
(Asteraceae); Brachycereus y Jasminocereus (Cactaceae)
y Sicyocaulis (Cucurbitaceae) (McMullen, 1999).
Desafortunadamente, de toda esta
riqueza natural y particular endemismo, más del 20% de plantas
están categorizadas como especies en peligro de extinción
(EN, 21 especies) o en peligro crítico de extinción
(CR, 13 especies) de acuerdo a los criterios de la Unión
Internacional para la Conservación de la Naturaleza (UICN)
publicados a finales del 2001 (Tye, 2002).
En este contexto, la
micropropagación resulta una estrategia interesante puesto que
permite trabajar con especies cuyas poblaciones naturales son muy
limitadas en las cuales la colección de semillas puede ser una
acción que va en detrimento de la sobrevivencia en forma
silvestre (Clemente, 1999).
Materiales y Métodos

Muestras de Darwiniothamnus
alternifolius fueron colectadas en el volcán Sierra Negra,
al sur de la Isla Isabela. En esta misma Isla se colectaron
especimenes de Scalesia affinis de Puerto Villamil donde la
especie no se encuentra en peligro crítico de extinción.
Además se ha trabajado con muestras de D. tenuifolius
cuyo estado es NT (casi amenazada) (Valencia, 2000) colectadas en la
Isla Santa Cruz. Todo el material vegetal colectado se almacenó
previo a su manipulación a 4ºC (Sands,
2003).
Explantes y Desinfección
Se ha
trabajado con tres tipos de explantes: capítulos (c),
flósculos (f) y yemas (y). Los explantes fueron lavados
superficialmente con agua destilada estéril y 1-2 gotas de
Tween 20. En cámara de flujo laminar se lavaron con etanol 70%
por un minuto y tres enjuagues con agua destilada estéril.
Posteriormente se aplicaron para cada explante tres diferentes
tratamientos de desinfección: d1. NaOCl 3% (v/v) 5 min,
tres enjuagues con agua destilada estéril, d2. NaOCl 3% +
ácido láctico 1.4% (v/v) 5 min, d3. NaOCl 3%, tres
enjuagues en agua destilada estéril, H2O2
10 vol. 1 min y tres enjuagues con agua destilada estéril.
Al terminar el último
enjuague los capítulos se disecan en 4 o 6 partes de acuerdo a
su tamaño, y se extraen además flósculos
individuales. Los tallos son disecados en porciones de 1-2 cm dejando
de una a tres yemas por segmento dependiendo del material, y
eliminando los extremos que presenten tejido afectado por los
desinfectantes.
Los explantes fueron finalmente
sembrados en tubos de ensayo de 150 x 25 mm conteniendo 10 ml de
medio MS (Murashige-Skoog, 1962) sin reguladores de crecimiento. El
pH fue ajustado a 5.8 utilizando 1 N NaOH/ 1 N HCl
antes de autoclavar a 15 PSI durante 15 minutos y se adicionó
3% de sacarosa y 0.7% de agar. Se utilizaron cuatro tubos por
tratamiento con seis repeticiones para D. alternifolius y S.
affinis, y tres repeticiones para D. tenuifolius.
Finalmente se transfierieron los tubos al cuarto de crecimiento
mantenidos a 25ºC, un fotoperíodo de 16 h con lámparas
fluorescentes de luz blanca e inspeccionados diariamente.
Resultados y Discusión

Los tratamientos desinfectantes
permitieron alcanzar un alto número de flósculos libres
de contaminación sobre todo para las dos especies de
Darwiniothamnus (tabla 1). Estos explantes fueron transferidos
a medio MS con diferentes concentraciones de benzyl amino purina
(BAP) y ácido indol acético (IAA) sin encontrarse
desarrollo en ninguno de los tratamientos después de ocho
semanas de observación.
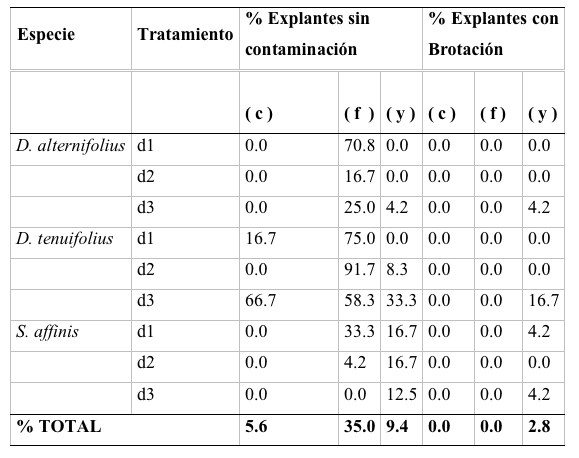
Tabla 1.
Porcentaje de explantes libres de contaminación y porcentaje de brotación de los explantes sembrados para las tres especies.
En cuanto a los capítulos
y yemas, ambos tipos de explantes presentaron
porcentajes de contaminación altos (figura 1), que impidieron
un desarrollo posterior aun al colocarlos en soluciones con
reguladores de crecimiento. La única excepción a este
resultado se dio con el material obtenido de D. alternifolius
sin contaminación que desarrolló brotes al colocarlo en
medio MS con 0.5mg L-1 BAP y 0.5mg L-1 IAA.
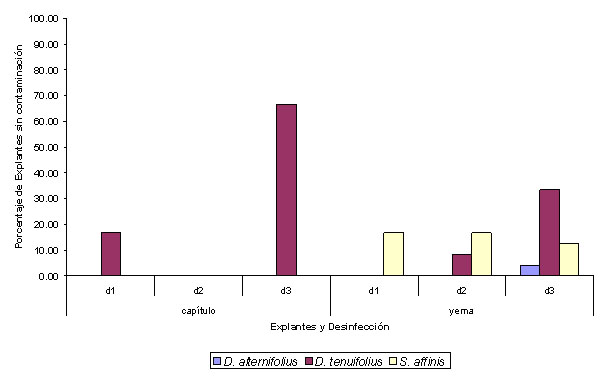
Figura 1.
Porcentaje de explantes libres de contaminación luego de la
aplicación de tres diferentes tratamientos de desinfección
en tres tipos de explantes de D. alternifolius, D. tenuifolius y S.
affinis.
A pesar de la contaminación
se observaron brotes a partir de explantes de yemas aun estando en
medio MS sin reguladores de crecimiento (figura 2) pero finalmente
murieron. En muchos de los explantes libres de contaminación
se presentó exudación de fenoles en un alto porcentaje,
principalmente en capítulos.
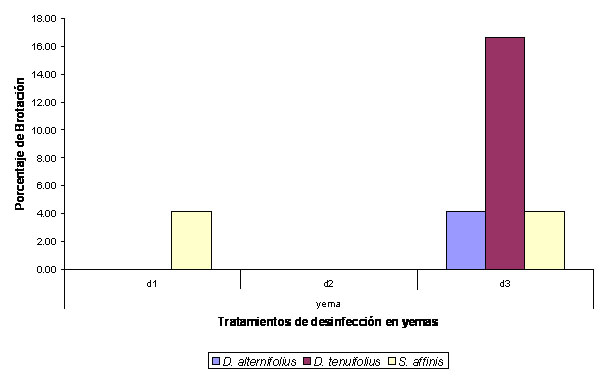
Figura 2.
Porcentaje de brotación observado en yemas de D.
alternifolius, D. tenuifolius y S. affinis
sembrados en MS sin reguladores de crecimiento.
En base a los
resultados obtenidos hasta el momento, se continuará con la
evaluación de yemas en principio de D. tenuifolius
buscando un tratamiento desinfectante que permita obtener mayor
cantidad de material vegetal para las siguientes etapas de brotación
y enraizamiento y aplicarlas a las otras dos especies. Los
tratamientos actualmente en evaluación tienen una menor
concentración de hipoclorito de sodio y un mayor tiempo de
exposición de los explantes al desinfectante. Además,
se ha añadido 5 gotas de Tween 20 a todos los tratamientos
para ayudar a romper la tensión superficial del agua y
aumentar así el contacto con el tejido vegetal (Kyte, 1996).
Para
contrarrestar el fenómeno de la fenolización se añadió
al medio MS 0.1 % de carbón activado por su capacidad de
adsorción de sustancias obteniéndose resultados
positivos (George, 1993). Adicionalmente, previa a la desinfección
se realizará una inmersión en sustancias antioxidantes
que pueden ser útiles en la prevención de
polimerización de quinonas reduciendo la posibilidad de
reacción con proteínas en el medio de cultivo (Crompton
& Preece, 1986).
Conclusiones

- El medio MS permite el
desarrollo de brotes en explantes de yema incluso sin reguladores de
crecimiento por lo que es un medio adecuado para trabajos de
micropropagación con estas especies.
- La adición
de 0.5 mg L-1IAA y 0.5 mg L-1 BAP en el medio
MS promueve el desarrollo de múltiples brotes a partir de una
yema axilar en D. alternifolius.
- El medio MS con diferentes
concentraciones de IAA y BAP no ha promovido crecimiento activo en
explantes de flósculos.
Agradecimientos

Al Parque Nacional Galápagos,
Concepto Azul y Ecociencia por el apoyo tanto financiero como
logístico para la realización del presente trabajo.
Referencias

Clemente, M.
1999. In Vitro Culture and Plant Conservation. In: B.G. Bowes (Ed.) A
Color Atlas of Plant Propagation and Conservation. Manson
Publishing Ltda, London. pp. 224.
Crompton M.E &
J.E. Peerce 1986 Exudation and explant establishment. I.A.P.T.C.
Newsletter 50: 9-18.
George, E.
1993. Plant Propagation by Tissue Culture. Second/Ed. Exegetic
Ltda., Edington, England.
Kyte, L. &
J. Klein. 1996. Plants from Test Tubes. An Introduction to
Micropropagation. Tercera/Ed. Timber Press, Portland, Oregon.
McMullen, C.K. 1999. Flowering
Plants of the Galapagos. First/Ed. Cornell University Press, Ithaca,
New York.
Murashige, T.;
M. Serpa, & J.B. Jones. 1974. Clonal multiplication of Gerbera
trough tissue culture. In D. Hurtado & M. Merino (Eds.).
Cultivo de Tejidos Vegetales. Editorial
Trillas, Mexico DF. pp. 15-30.
Sands, R. J.;
N.R. Brown & A. Koutoulis. 2003. Micropropagation of two
threatened Tasmanian species of Calocephalus (Asteraceae),
with comments on phenotypic plasticity. Australian Journal of
Botany 51: 415-420.
Tye, A. 2002. Revisión del
Estado de Amenaza de la Flora Endémica de Galápagos. In
"Informe Galápagos 2001-2002". Fundación
Natura - WWF, Quito, Ecuador. pp. 116-122
Valencia, R.; N. Pitman; S.
León-Yánez & P.M. Jørgensen (Eds). 2000.
Libro rojo de las plantas endémicas del Ecuador.
Herbario QCA, Pontificia Universidad Católica
del Ecuador, Quito.


